胡桃坂 仁志
早稲田大学 理工学術院 教授
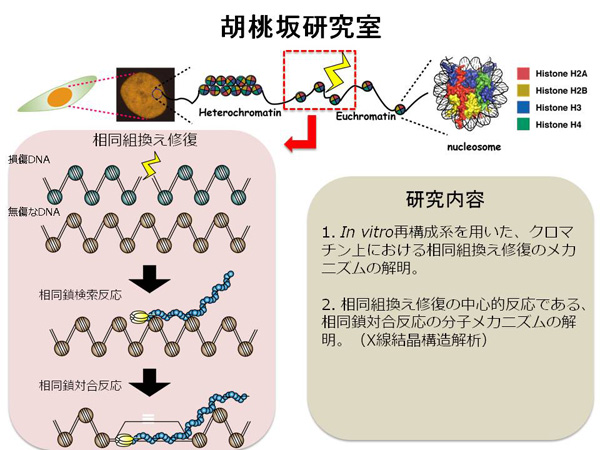
当研究室では、相同組換えによる二重鎖DNA損傷修復のメカニズムの解明を目標に研究に取り組んでいる。遺伝情報を担うDNAは、細胞内代謝で生じる化合物や紫外線、放射線などにより、恒常的に損傷を受けている。特に、放射線が原因となって引き起こされる二重鎖DNA切断損傷は、速やかに修復されなければ、染色体異常を引き起こし、細胞死やがんの要因となる。生物は、この重篤な損傷を正確に修復するために、相同組換え修復を進化させてきた。相同組換え修復では、無傷のDNA領域から損傷部位と相同な配列を探索し、その情報を用いて修復することで、二重鎖切断損傷を極めて正確に修復する(図)。ヒトをはじめとする真核生物では、DNAは核の中でコアヒストンタンパク質に巻き付き、さらに高度に凝集されたクロマチンと呼ばれる構造体を形成するが、当然ながら相同組換え修復もそのクロマチン上で行われる(図)。クロマチンは試験管内では一般的に修復反応を阻害することが明らかにされている、一方で、細胞では極めて効率的な修復反応が行われている。しかし、クロマチン上で効率的に相同組換え修復を行うメカニズムについてはほとんど明らかになっていない。当研究室では、クロマチンにおける相同組換え修復のメカニズムを明らかにするために、精製したリコンビナントタンパク質を用いて、クロマチンを試験管内再構成し、再構成クロマチンを用いた相同組換え反応の解析を行っている。また、相同組換え修復の中心反応は、無傷のクロマチンから、損傷部位と相同な配列を探索する「相同鎖検索」であるが(図)、この重要な反応を原子レベルで明らかにするために、当研究室ではX線結晶構造解析により、クロマチン上における相同組換え中間体の構造解析研究も推進している。基盤形成事業においては、当研究室は上述のように生化学的、構造生物学的手法を駆使して、相同組換え修復のメカニズムの解明を目指した多角的な研究を推進する。
25年度の計画:
紫外線や放射線などの細胞ストレスによるDNA損傷は、正常な細胞では速やかかつ正確に修復される。このDNA損傷修復機構の破綻は、未修復の二重鎖DNA切断の蓄積を引き起こし、染色体異常を伴う発がんの主要な原因の1つとなる。二重鎖DNA切断損傷は、呼吸に起因する活性酸素やDNA複製のエラーなどによっても日常的に引き起こされている。胡桃坂は、このような細胞ストレスによるDNA損傷の修復機構を明らかにするために、DNA修復反応のin vitro系を構築して生化学的および構造生物学的手法により研究を行う。平成25年度では、これまでに構築した紫外線や放射線に起因するDNA切断損傷のin vitro系修復系を用いて、既知の因子によるDNA組換え修復反応の素過程の解析を行う。並行して、DNA組換え修復に関わる未知の因子の同定およびその機能解析も行う。