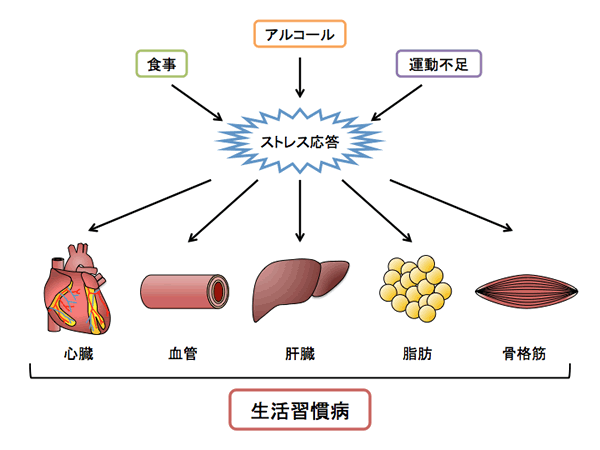
食生活の欧米化と運動不足による肥満を基盤とするメタボリックシンドロームや2型糖尿病は、心筋梗塞や脳梗塞などの心血管イベントを誘導する主要な要因であるため、超高齢化社会における健康寿命の延伸を脅かす重篤な疾患と考えられている。しかしながら、その発症は遺伝的な要因のみでは説明できず、多様な生活環境に大きく左右されることから、未だ有効な予防法もなく、罹患者数は増加の一途を辿っている。このような背景に基づき、本研究班では、環境や食など常に我々が曝され続けている様々なストレスに対する感受・応答システムの破綻が、肥満や糖尿病に代表される生活習慣病の発症・進展に密接に関わっていることに着目し、ストレス制御に立脚した病態の新しい予防法、診断法および治療法の開発に繋がる研究基盤を確立することを目指す。この実現のために、ストレスの種類、強弱、時刻・タイミング、加算・加重などの要素を人為的に変え作出する新しい疾患モデルを開発し、その個体および細胞レベルでの詳細な解析により病態の成り立ちを分子レベルで理解することで、新たな知見に基づいた評価診断法や治療法の開発に取り組む。具体的には、病態誘導食の質的・量的な変化のみならず、投与のタイミングと投与量バランスも加味した新しい病態モデル動物を作成し、これらの病態の発症・進展を定量的に評価できるバイオマーカーを、遺伝子、タンパク質および低分子の網羅的解析法を用いて同定する。また、加齢による全身臓器、特に脂肪、肝臓や膵臓などの代謝臓器のみならず、代謝制御機構の破綻により新たな病態が形成される心血管系にも焦点を当て、これらの臓器の機能・構造的リモデリングが及ぼすストレスに対する感受性や応答性の変化についても解析を行う。一方、上記疾患モデル動物より単離した細胞および疾患関連遺伝子異常の患者より樹立したiPS細胞から分化誘導した細胞を用い、時間軸を考慮したストレス感受・応答性変化にかかわるタンパク質修飾やエピジェネティック制御機構を明らかにすることで、これらを標的としたストレス制御の評価診断法や治療法の開発に繋がる研究基盤を確立する。